A partir del desarrollo en la ciencia de materiales, se han buscado nuevas formas
terapéuticas para tratar las enfermedades de manera eficaz y segura. Según datos de
la OMS, la resistencia a los antimicrobianos (RAM) pone en peligro la eficacia de
la prevención y el tratamiento de una serie cada vez mayor de infecciones por virus,
bacterias, hongos y parásitos. Además, supone una amenaza cada vez mayor para la salud
pública mundial y requiere medidas por parte de todos los sectores del gobierno y
la sociedad.
El éxito de la cirugía mayor y la quimioterapia cada vez se verá más comprometido
en ausencia de antibióticos eficaces. Por otro lado, la prolongación de las enfermedades,
la necesidad de más pruebas y la utilización de fármacos más caros aumentan el costo
de la atención sanitaria a los pacientes con infecciones multirresistentes. Se estima
que cada año cerca de 480,000 personas presentan tuberculosis multirresistente, y
la farmacorresistencia empieza a complicar también la lucha contra el vih y el paludismo
(World Health Organization, 2018).
Algunas de las potenciales ventajas de las nanopartículas (NPs), para luchar contra
las
enfermedades infecciosas causadas por microrganismos, es que no generan resistencia
en éstos, pudiendo reducir los efectos secundarios en el paciente (Jan et al., 2014; Kalyani et al., 2015; Mamonova et al., 2015).
Sin embargo, es de considerar que falta mucha investigación para poder entender cómo
actúan
las NPs y así poder diseñar mejores terapias. Se ha visto que la actividad de
las
nanopartículas depende del tamaño y de la forma de las mismas; por lo que se
requiere investigación activa de los materiales a escala nanométrica para llevar
a
cabo su diseño. En los últimos tiempos se ha realizado mucha ciencia básica y
aplicada alrededor de diversos óxidos metálicos con diferentes formas y tamaños
para
su posible aplicación en catálisis, como semiconductores, sensores, en liberación
controlada de fármacos y como agentes antimicrobianos.
Las propiedades físicas y químicas de las NPs de óxidos metálicos permiten su interacción
con
sistemas biológicos, lo cual se ha vuelto de vital importancia debido a la creciente
resistencia de bacterias sobre todo Gram-negativas. Dentro de estas propiedades
se
encuentran la forma, tamaño, rugosidad, potencial zeta y recubrimientos, entre
otros
(Mamonova et al., 2015;
Wang et al., 2017). La
actividad antimicrobiana que presentan las nanoestructuras de dichos óxidos podría
tener una aplicación a nivel terapéutico principalmente, pero también puede
extenderse a la industria alimenticia, a la purificación de agua y a la industria
textil.
Los óxidos metálicos en general y en particular los óxidos formados por metales de
transición
son compuestos con propiedades electrónicas únicas, la mayoría de los fenómenos
magnéticos involucran a este tipo de óxidos. Además, sus nanoestructuras, debido
a
sus dimensiones de unos cuantos nanómetros y a su gran superficie específica,
resultan candidatos ideales para interactuar con las bacterias. De tal manera,
las
NPs de óxidos metálicos se han convertido en una alternativa para combatir bacterias
resistentes a la acción de antibióticos (Raghunath y
Perumal, 2017). En particular, se ha informado que las NPs de óxido de
titanio (TiO2), óxido de cinc (ZnO), óxido cúprico (CuO), la magnetita
(Fe3O4) y el óxido de magnesio (MgO) presentan importantes
propiedades antimicrobianas, las cuales dependen en gran medida de su composición
química, forma y tamaño.
Finalmente, también es importante considerar que los cationes presentes en la superficie
de
las NPs formadas por óxidos metálicos, son ácidos de Lewis con valencias insaturadas
que podrían formar enlaces de tipo covalente dativo, con bases de Lewis (grupos
nitrogenados y oxigenados) presentes en los aminoácidos y polisacáridos
constituyentes de la pared celular. Dicha interacción también podría generar la
lisis de la pared celular.
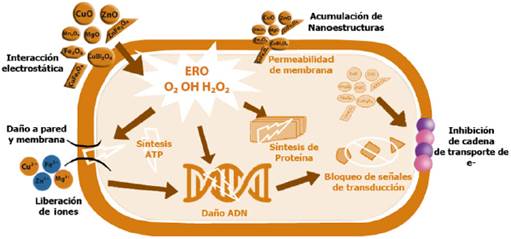
Por todo lo anterior, es importante tener en cuenta que existen diversos mecanismos
que pueden
estar involucrados en la actividad antimicrobiana de las NPs de los óxidos
metálicos.
Mecanosíntesis
El término mecanoquímica se refiere a las reacciones químicas que involucran reactivos en cualquier estado
de agregación, pero comúnmente se usa para reacciones sólido-sólido, en donde la energía
necesaria para llevar a cabo la reacción, involucra un proceso o tratamiento mecánico
(Heinicke et al., 1984). Este método se ha empleado en los últimos años para sintetizar materiales a partir
de reactivos en estado sólido, que a temperaturas habituales de trabajo no muestran
la reactividad necesaria para su formación, o bien, para la preparación de compuestos
que, en condiciones normales de presión y temperatura, son metaestables o no pueden
ser obtenidos por métodos de síntesis convencionales. Se ha comprobado que la activación
mecanoquímica de sólidos cambia su reactividad, debido a la acumulación de defectos
en situación de no equilibrio, lo cual repercute en la disminución de las energías
de activación para que se lleven a cabo algunas reacciones químicas (Gaffet et al., 1999). La acción mecánica que se ejerce sobre los reactivos permite llevar a cabo una
verdadera reacción química (mecanosíntesis) que hace posible obtener nuevos compuestos,
con dimensiones nanométricas. En general, la energía mecánica que se aporta a los
reactivos en estado sólido puede acumularse en la deformación plástica de los cristales,
produciendo defectos cristalinos que, en consecuencia, producen regiones de especial
reactividad química que facilitan el desarrollo de los procesos en fase sólida. Según
el sistema y las condiciones de activación, pueden producirse reacciones en fase sólida
durante el tratamiento mecánico a temperatura ambiente y/o pueden generarse cambios
estructurales, reduciéndose la temperatura necesaria de ciertas reacciones.
La mecanosíntesis ha despertado el interés de diversos grupos de investigación en
nanomateriales principalmente debido a su sencillez y su bajo impacto ambiental.
En nuestro grupo de investigación hemos llevado a cabo la obtención de nanoestructuras
de
diferentes óxidos metálicos por un proceso que involucra la molienda de las
sales metálicas de partida, generalmente cloruros o acetatos, en presencia de
una base (NaOH o KOH), el producto obtenido se lava con agua y posteriormente
con acetona, separando en cada ocasión por centrifugación. En algunos casos no
ha sido necesario llevar a cabo un tratamiento térmico posterior, y en otros,
se
han llevado a cabo tratamientos térmicos por 400, 600 y 800 ºC, durante 2 horas.
En la Figura 2 se presenta el esquema
general de síntesis de las NPs de diferentes óxidos metálicos obtenidos en
nuestro grupo de investigación.
Figura 2
Esquema general de la metodología llevada a cabo para obtener diferentes nanoestructuras
de óxidos metálicos.
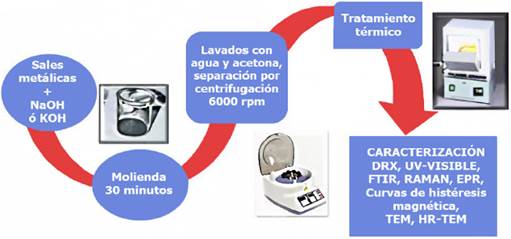
Fuente. Imagen de metodología proporcionada por América Vázquez Olmos.
Todas las nanoestructuras han sido caracterizadas por difracción de rayos-X en polvo,
espectroscopías de absorción electrónica UV-visible, infrarrojo por transformada
de Fourier (FTIR), dispersión Raman, resonancia paramagnética electrónica (EPR),
microscopía electrónica de transmisión (TEM) así como microscopía electrónica
de
transmisión de alta resolución (HR-TEM). La caracterización magnética de dichas
nanoestructuras también se ha llevado a cabo. En la Figura 3 se presentan algunas micrografías obtenidas por
HR-TEM de las NPs de los óxidos obtenidos en nuestro grupo de investigación.
FIGURA 3
Micrografías obtenidas por HR-TEM, de algunos de los óxidos nanoestructurados obtenidos
por mecanosíntesis.

Fuente. Imágenes de América Vázquez Olmos y colaboradores.
A continuación se presenta una breve revisión sobre las propiedades antimicrobianas,
informadas en la literatura, de los siguientes sistemas nanoestruturados; CuO, CuBi2O4, ZnO, Mn3O4, Fe2O3, CuFe2O4, ZnFe2O4 y MgO, los cuales han sido obtenidos en nuestro grupo de investigación, empleando
la aproximación mecanoquímica.
Nanoestructuras de CuO
El cobre es un conocido agente antimicrobiano desde hace varios siglos. Se ha utilizado
de diversas formas para evitar la propagación de diferentes enfermedades desde el
Egipto antiguo, pasando por el Imperio romano y hasta en la Segunda Guerra Mundial
(Prado et al., 2012; Vincent et al., 2016). Sin embargo, el metal no sólo puede ser tóxico para los microrganismos, también
para los humanos y el ambiente. Tomando en cuenta su toxicidad, se han estudiado de
manera intensiva un gran número de materiales basados en el cobre, para poder controlar
su liberación al medio ambiente (Prado et al., 2012). En ese sentido, el óxido cúprico CuO ha resultado ser un compuesto muy popular
debido a su estabilidad, larga vida útil, así como a sus diversas aplicaciones. El
CuO se encuentra en la naturaleza como el mineral tenorita, cristaliza en forma monoclínica
y es un semiconductor tipo p, con un band gap estrecho de 1.2 eV.
En los últimos años las nanopartículas y nanocompositos de CuO han sido ampliamente
estudiados por su efecto antimicrobiano y son el sistema más utilizado a nivel
comercial; en textiles, como biocidas y en pinturas, debido a dicho efecto
(Hou et al., 2017).
Se ha probado que tiene efecto antimicrobiano frente a cepas de
Escherichia coli, Enterococcus faecalis,
Pseudomonas aeruginosa, Klebsiella
pneumoniae, Staphylococcus aureus y
Bacillus subtilis, entre otras (Katwal et al., 2015); mostrando una
actividad de 20 a 90 veces mejor que la observada en CuO en
bulk (Hou et
al., 2017). Diferentes estudios llevados a cabo para
determinar el mecanismo de acción de las NPs de CuO, revelan que éstas
interactúan con la pared celular bacteriana, favoreciéndose la penetración de
éstas y a su interacción con el material genético. Esto genera una serie de
daños y desorganización celular, llevando a la muerte de la bacteria. La
interacción que se lleva a cabo dependerá del diámetro de las nanopartículas,
la
modificación de su superficie, la vía de exposición y la posible liberación de
iones Cu2+ (Hou et
al., 2017).
Nanoestructuras de
CuBi2O4
El óxido de cobre y bismuto, CuBi2O4, se encuentra en la naturaleza
como el mineral Kusachiita y es un material semiconductor tipo p, con una
energía de brecha prohibida o band gap de 1.5 - 1.8 eV,
cristaliza en forma tetragonal. Hasta ahora las principales aplicaciones del
CuBi2O4 son en la degradación de algunos colorantes
contaminantes del agua y como microbicida (Elaziouti et al., 2016; Wen-da
et al., 2016; Zhu et al., 2016). Un estudio reciente señala que
microestructuras de CuBi2O4 demostraron tener una buena
acción fotocatalítica en la conversión de energía y tener un buen efecto
antimicrobiano frente a cepas de E. coli, observándose una
reducción del 93.3% en su densidad óptica después de una irradiación de luz
led (10 mW/cm2) (Zhu et al., 2016). Las NPs de
CuBi2O4 resultan un material prometedor como agente
antimicrobiano.
Nanoestructuras de ZnO
El óxido de zinc ZnO es un compuesto ampliamente conocido por sus propiedades
antimicrobianas. Es un semiconductor tipo n con un band gap de
3.3eV cuya estructura cristalina puede ser hexagonal (tipo wurtzita) o cúbica
(blenda de zinc), siendo la wurtzita la más común. Las NPs de ZnO pueden adoptar
una gran variedad de morfologías como son; anillos, hélices, cinturones,
alambres y flores, entre otros (Król et
al., 2017; Wang,
2004). Las nanopartículas de ZnO actúan como agentes antimicrobianos
a través de diversos mecanismos, siendo el más importante la generación de
especies reactivas de oxígeno (Kaftelen
et al., 2012) al interior de la célula. Se ha
propuesto que las NPs de ZnO pueden actuar para generar la muerte celular, o
bien, como fuente de iones de Zn2+, cuyo exceso genera una alteración
del metabolismo celular. Algunas especies reportadas como susceptibles a las
NPs
de ZnO son; S aureus, S. epidermidis,
Streptococcus pyogenes, Enterococcus
faecalis (Santhoshkumar et
al., 2017), Bacillus subtilis,
Escherichia coli y Klebsiella pneumoniae
(Król et al., 2017).
Estas bacterias son de interés clínico, ya que pueden generar infecciones
intra-hospitalarias ocasionando cuadros infecciosos graves y algunas cepas se
encuentran en el agua o comida, por lo que las NPs de ZnO pueden tener una
posible aplicación en diversas industrias.
Nanoestructuras de
Mn3O4
El tetróxido de trimanganeso, Mn3O4, es un óxido mixto de manganeso
(Mn(II)Mn(III)2O4) que cristaliza en forma cúbica y es una espinela normal. Se
presenta en la naturaleza como el mineral hausmanita. Las propiedades
antimicrobianas de las NPs de Mn3O4 han sido poco
estudiadas. Se ha informado un efecto moderado de dichas NPs frente a cepas del
Vibrio cholerae, Shigella sp.,
Salmonella sp., y Escherichia coli (Chowdhury et al., 2009).
Por otro lado, se ha evaluado el efecto de las NPs de
Mn3O4 frente a cepas de E. coli y
S. aureus a través de ensayos de microdilución (Azhir et al., 2015). Los
resultados de las concentraciones mínimas inhibitorias (CMI) indicaron que la
bacteria E. coli fue más sensible a la acción de las NPs de
Mn3O4. Se observó que el efecto inhibitorio se
incrementa conforme aumenta la concentración de NPs de
Mn3O4, lo cual podría deberse a las diferentes
características de las superficies de las células bacterianas y su interacción
con las NPs, es decir, el mecanismo de acción podría enfocarse en la pared de
la
membrana bacteriana.
Nanoestructuras de
Fe2O3
El óxido de hierro (III) es un óxido muy estable, que cristaliza en forma hexagonal
y se
encuentra en la naturaleza como el mineral hematita
α-Fe2O3. Las nanoestructuras de este óxido adoptan
diferentes formas como son; nanoalambres, nanotubos, nanoesferas, etcétera
(Tadic et al.,
2017). Si bien su síntesis ha sido ampliamente estudiada, no así su
posible efecto antimicrobiano. Se ha informado sobre su efecto bactericida
contra E. coli y S. aureus, en donde se
observa un incremento de tal efecto, conforme aumenta la concentración de las
NPs de Fe2O3 (Rufus
et al., 2016). También se ha visto un efecto
bactericida a P. aeruginosa con una concentración mínima
inhibitoria de 0.06mg/L (Irshad et
al., 2017). Otro estudio informa sobre la actividad
bactericida de la hematita nanoestructurada contra una variedad de bacterias
Gram-positivas y Gram-negativas; P. aeruginosa, S.
aureus, K. pneumoniae, Lysinibacillus
sphaericus y Bacillus safensis (Muthukumar et al., 2017);
proponiendo incluso algunos mecanismos de acción dependiendo de la actividad
observada en cada etapa del crecimiento de la bacteria en cuestión. Incluso se
ha llegado a determinar un efecto bactericida de NPs de
Fe2O3 contra S. epidermidis (Groiss et al., 2017).
A partir de sus propiedades se ha propuesto su posible aplicación en la remediación
del ambiente y del agua, así como en el área biomédica, debido a los diferentes estudios
de citotoxicidad que se han llevado a cabo. (Tadic et al., 2017).
Nanoestructuras de ferrita de cobre
(CuFe2O4)
y de ferrita de cinc
(ZnFe2O4)
Hasta ahora no se ha llevado a cabo mucha investigación alrededor de la actividad
antimicrobiana de ferritas, a no ser por la ferrita de hierro, la magnetita Fe3O4 (Kefeni et al., 2017). Sin embargo, ya que se ha observado que los óxidos de hierro (Fe3O4, Fe
2
O3), de cobre (CuO) y de cinc (ZnO) presentan actividad antimicrobiana es factible pensar
que la ferrita de cobre, CuFe2O4 y la ferrita de cinc ZnFe2O4, puedan presentar actividad antimicrobiana frente a cepas de diferentes bacterias
Gram-positivas y Gram-negativas.
En particular NPs de ZnFe2O4 han mostrado buena actividad
antimicrobiana contra S. aureus, B. subtilis y
E. coli, siendo su actividad muy comparable con la
estreptomicina (Mandal et al.,
2016). Por otro lado, no se encuentran informes en la literatura
acerca de la actividad antimicrobiana de NPs de CuFe2O4.
Debido a la falta de información en relación con estas ferritas, y en especial
a
la de cobre, es que se quiere llevar a cabo el estudio de su posible actividad
antimicrobiana. Las NPs de dichas ferritas podrían servir como acarreadores de
iones metálicos de cobre o de cinc, presentando efectos tóxicos contra las
bacterias.
Nanoestructuras de MgO
El óxido de magnesio MgO, se presenta en la naturaleza como el mineral periclasa (Rankin, 2009). Se ha informado sobre la
actividad antibacteriana del MgO contra bacterias Gram-positivas y
Gram-negativas. Se ha informado que la actividad antimicrobiana del MgO
micrométrico, se debe a la presencia de oxígeno activo como superóxido
(O2-), en la superficie de las partículas de MgO (Sawai et al., 2000; Sawai, 2003; Sawai y Yoshikawa, 2004). Por otro lado, se ha propuesto
que las NPs de MgO pueden dañar la membrana celular causando la pérdida de
contenidos intracelulares y provocando la muerte de las células bacterianas
(Jin y He, 2011). Se ha atribuido la
generación de especies reactivas de oxígeno a la alcalinidad de la superficie
de
las NPs de MgO (Yamamoto et
al., 2010). Se ha evaluado la actividad antibacteriana de
NPs de MgO contra bacterias Gram-negativas; E. coli y
P. aeruginosa (500 y 1000 μg/mL) y en una bacteria
Gram-positiva; S. aureus (1000 μg/mL) (Krishnamoorthy et al., 2012). Las NPs de
MgO potenciaron la peroxidación de lípidos inducida por ultrasonido en la
membrana liposomal. En este caso el mecanismo de acción podría estar asociado
con la presencia de defectos, o bien a la falta de oxígeno en la superficie de
la nanopartícula, conduciendo a la peroxidación lipídica y la generación de
especies reactivas de oxígeno (Krishnamoorthy et al., 2012). El
efecto antibacteriano y el mecanismo de acción de NPs de MgO contra cepas de
Campylobacter jejuni, E. coli y
Salmonella enteritidis ha sido estudiado (He et
al., 2016). En este caso se observó que la permeabilidad de la
membrana de las bacterias, después de la exposición a las NPs de MgO, se vio
comprometida, encontrándose la presencia de peróxido de hidrógeno que
subsecuentemente causaría muerte celular. Cepas de P.
aeruginosa y S. aureus frente a NPs de MgO
mostraron una mayor zona de inhibición en S. aureus que en
P. aeruginosa (Bindhu
et al., 2016). Basándose en trabajos previos,
los autores señalan que la acción bactericida de las nanopartículas de MgO se
puede deber a la unión del oxígeno superficial a las bacterias. A medida que
aumenta el área superficial de las partículas, aumenta la concentración de iones
oxígeno en la superficie, lo que da como resultado una destrucción más efectiva
de la membrana citoplásmica y de la pared celular de las bacterias.